今回は、「化学反応式と量的関係」についての話題です。。。
では、さっそく、考えてみましょう。
問題
標準状態において、7.5gのエタンC$_2$H$_6$ と22.4$\ell$ の酸素 O$_2$ を
混合し、これに点火して、完全に燃焼させた。次の各問いに答えよ。
原子量は H$=1.0$、C$=12$、O$=16$、アボガドロ定数は $6.0\times10^{23}$ とする。
- この反応を化学反応式で表せ。
- 反応前のエタンの物質量(mol) と含まれる水素原子の数を求めよ。
- 反応せずに残った気体は何か。また、その質量は何 g か。
- 生成した二酸化炭素は標準状態で何 $\ell$ か。
- 2C$_2$H$_6$ $+$ 7O$_2$ $\longrightarrow$ 4CO$_2$ + 6H$_2$O //
- エタンの分子量 C$_2$H$_6 = 30$ より、
C$_2$H$_6$ の1molあたりの質量は 30 g / mol 。
エタン7.5gの物質量は、$\dfrac{7.5}{30}=0.25$ (mol)。 //
また、エタン1分子中には、H が 6 個含まれるから、 H 原子の数は、$0.25\times6\times6.0\times10^{23}=9.0\times10^{23}$ 個。 // - 反応式の係数比より、
$$\mathrm{C}_{2}\mathrm{H}_6 : \mathrm{O}_2 = 2:7~~ (~\mathrm{mol}比~)$$
で反応する。
0.25molのC$_{2}$H$_{6}$と1.0molのO$_2$からは、C$_{2}$H$_{6}$ が全部反応する。
O$_2$は$0.25\times\dfrac{7}{2}=0.875$ (mol) が反応し、$1.0-0.875 =0.125$ mol が残る。
つまり、反応せずに残った気体は「酸素」である。//
その質量は、O$_2$=32 g/mol より、 $$0.125\times32=4.0~(g) //$$ - 反応式の係数比より、生成したCO$_2$の物質量は反応したC$_2$H$_6$の物質量の$(\dfrac{4}{2}=)~~ 2$ 倍である。
よって、 $$0.25\times2\times22.4=11.2 \approx 11 \ell //$$
問題
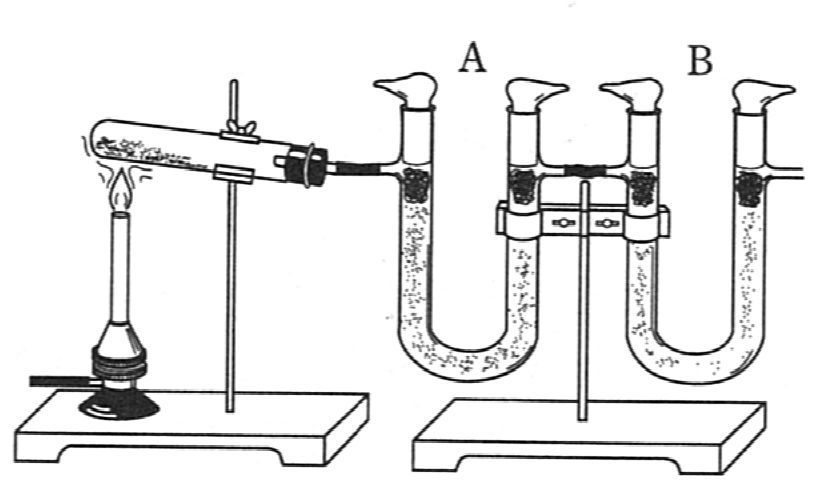
図のように炭酸水素ナトリウムと炭酸ナトリウム十水和物の 混合物を加熱して、 発生する気体を吸収管に吸収させたところ、 吸収管Aでは360mg、Bでは440mg の質量の増加が観察された。 この結果から最初の混合物中の炭酸水素ナトリウムと炭酸ナトリウム十水和物の 物質量比はいくらか。
ただし、吸収管Aには塩化カルシウム、Bにはソーダ石灰が入っている。 また、 H$=1.0$、C=12、O=16 とする。

図のように炭酸水素ナトリウムと炭酸ナトリウム十水和物の 混合物を加熱して、 発生する気体を吸収管に吸収させたところ、 吸収管Aでは360mg、Bでは440mg の質量の増加が観察された。 この結果から最初の混合物中の炭酸水素ナトリウムと炭酸ナトリウム十水和物の 物質量比はいくらか。
ただし、吸収管Aには塩化カルシウム、Bにはソーダ石灰が入っている。 また、 H$=1.0$、C=12、O=16 とする。
吸収管Aの塩化カルシウムCaCl$_2$には水分が吸収され、
吸収管Bのソーダ石灰(CaO+NaOHの混合物)には、CO$_2$が吸収される。
吸収されたH$_2$(=18)とCO$_2$(=44)の物質量は $$\mathrm{H}_2\mathrm{O}: \dfrac{360\times10^{-3}}{18}=2.0\times10^{-2}~(\mathrm{mol})$$ $$\mathrm{CO}_2: \frac{440\times10^{-3}}{44}=1.0\times10^{-2}~(\mathrm{mol})$$ である。
ここで、混合物中のNaHCO$_3$ を$x$ (mol) 、Na$_2$CO$_{3}\cdot$10H$_2$O を $y$ (mol) とおくとき、
2NaHCO$_3 \longrightarrow $ Na$_2$CO$_3$ + H$_2$O + CO$_2$
$~~~~~~x~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~\dfrac{x}{2}~~~~~\dfrac{x}{2}$
Na$_2$CO$_3\cdot$10H$_2$O $\longrightarrow$ Na$_2$CO$_{3}$ + 10H$_2$O
$~~~~~~y~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~10y$
より、 $$\frac{x}{2}+10y=2.0\times10^{-2} \cdots(ア)$$ $$\frac{x}{2}=1.0\times10^{-2} \cdots(イ)$$ (ア)、(イ)より、 $$\therefore x=2.0\times10^{-2} (\mathrm{mol})$$ $$\therefore y=1.0\times10^{-3} (\mathrm{mol})$$ よって、 $$\therefore x : y = 20 : 1 //$$
吸収されたH$_2$(=18)とCO$_2$(=44)の物質量は $$\mathrm{H}_2\mathrm{O}: \dfrac{360\times10^{-3}}{18}=2.0\times10^{-2}~(\mathrm{mol})$$ $$\mathrm{CO}_2: \frac{440\times10^{-3}}{44}=1.0\times10^{-2}~(\mathrm{mol})$$ である。
ここで、混合物中のNaHCO$_3$ を$x$ (mol) 、Na$_2$CO$_{3}\cdot$10H$_2$O を $y$ (mol) とおくとき、
2NaHCO$_3 \longrightarrow $ Na$_2$CO$_3$ + H$_2$O + CO$_2$
$~~~~~~x~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~\dfrac{x}{2}~~~~~\dfrac{x}{2}$
Na$_2$CO$_3\cdot$10H$_2$O $\longrightarrow$ Na$_2$CO$_{3}$ + 10H$_2$O
$~~~~~~y~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~10y$
より、 $$\frac{x}{2}+10y=2.0\times10^{-2} \cdots(ア)$$ $$\frac{x}{2}=1.0\times10^{-2} \cdots(イ)$$ (ア)、(イ)より、 $$\therefore x=2.0\times10^{-2} (\mathrm{mol})$$ $$\therefore y=1.0\times10^{-3} (\mathrm{mol})$$ よって、 $$\therefore x : y = 20 : 1 //$$
いかがでしたか。
理解は出来ましたか?
では、また次回にお会いしましょう。